
一种与凋亡(Apoptosis)、自噬(Autophagy) 及已明确的程序性坏死(Programmed Necrosis) 途径均存在显著差异的特定类型坏死性细胞死亡。
2025年2月6日,由上海交通大学医学院钟清团队联合中国科学院上海药物所李扬团队发表于 Nature Chemical biology 期刊的论文揭示了一种以钠过载为特征的新型细胞死亡形式,并将其命名为——钠过载细胞死亡 (Necrosis by Sodium Overload,NECSO)。(研究中使用了TargetMol的一系列产品哦~


钠死亡?
早在 2023 年 4 月,该研究团队于 Cell Death & Disease 期刊报道了一种可在特定癌细胞系中诱导强烈的免疫原性坏死细胞死亡的化合物——Necrocide 1(NC1)。

NC1 诱导的细胞死亡途径与当前已知的铁死亡、坏死性凋亡、焦亡等细胞死亡通路不同,其特征表现为钠离子过载,并依赖于单价阳离子通道 TRPM4,是一种独特的细胞死亡途径。在这项最新研究中,研究团队将这种细胞死亡途径命名为钠过载细胞坏死(Necrosis by Sodium Overload,NECSO)。
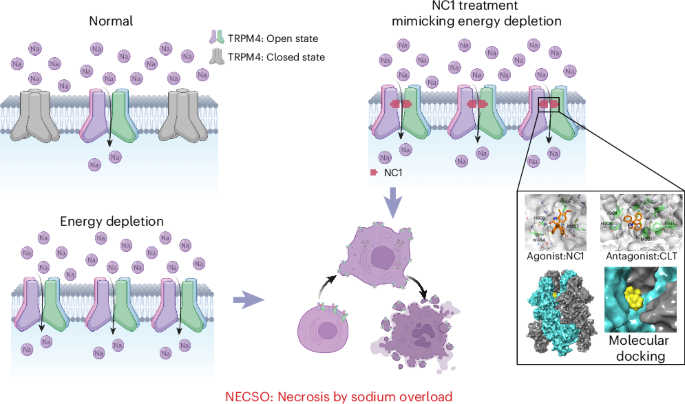
▲NECSO示意图
TRPM4 ——NECSO的关键因子
TRMP4 是一种钙激活的非选择性单价阳离子通道蛋白,在 NC1 诱导的 NECSO 过程中起关键作用。研究团队进行的全基因组 CRISPR-Cas9 筛选显示,在 NC1 处理后的抗性细胞库中,TRPM4 是与 NC1 作用最显著相关的基因。
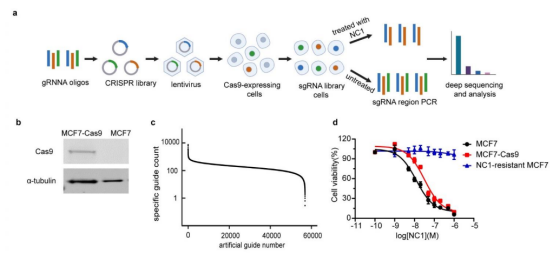
▲全基因组 CRISPR-Cas9 筛选策略示意图
进一步的实验验证了 TRPM4 在 NECSO 发生中的核心作用:
TRPM4-KO 细胞可完全抵抗 NC1 诱导的坏死,致使细胞存活率上升;
外源性表达TRMP4可恢复NC1诱导的坏死,同时,TRPM4 抑制剂 9-phenanthrol 也可抑制该过程;
TRPM4 的离子通道活性对于 NC1 诱导的坏死至关重要,无离子通透性的突变体 TRPM4-D984A 无法恢复 NC1 敏感性。
结合生化实验与电生理分析,研究揭示了 NC1 通过直接结合 TRPM4 并持续激活其离子通道功能,从而诱导 NECSO。并且,NC1具有高度特异性,仅在表达人源TRPM4 的细胞中诱导 NECSO,这一点也通过结构域交换实验和分子对接分析得到证实。
此外,研究发现在 NECSO 过程中,TRPM4 介导的 Na⁺ 超载是其核心机制。TRPM4 通过促进 Na⁺ 内流,导致一系列生理变化,如引发膜去极化、氯离子内流和渗透失衡,最终导致细胞坏死。

▲钠离子内流是NC1诱导细胞死亡的关键
TRPM4 此前被报道与缺血和脊髓损伤相关的 ATP 耗竭密切相关。研究团队推测,NECSO 可能也与能量耗竭存在联系,并进行了进一步实验。
通过在 Cos7 细胞中表达野生型 TRPM4 或突变体,并观察细胞在NC1 或 2-脱氧-D-葡萄糖(2DG)+ NaN3(能量耗竭处理)下的死亡情况。发现:
能量耗竭也能触发钠离子内流和坏死性细胞死亡,并与 NECSO 具有相似的遗传特征,且 TRPM4 在其中也起关键作用。这表明,NECSO 不仅仅是由 NC1 触发的一种细胞死亡模式,能量耗竭等其他生理或病理因素同样可能诱导 NECSO 发生。
NECSO 抑制剂
随后,研究鉴定了一系列能够抑制 NECSO 的小分子抑制剂。
1)TRPM4 的直接抑制剂
利用 TRPM4 的 NC1 结合口袋进行计算筛选,发现 克霉唑(CLT)通过疏水相互作用、范德华接触和氢键与 TRPM4 结合,作用于 S5 中的 M927、S6 中的 F931 和 S4 中的 H908 等残基。CLT 与 NC1 竞争 TRPM4 上的结合口袋,从而抑制 TRPM4 的激活和 NECSO。
CLT 的效力在 MCF7 细胞中进行了测试,其半最大有效浓度(EC50)为 4 µM。电生理学实验也确认了其对 TRPM4 的抑制作用。
2)FDA 批准药物库的筛选
通过对 FDA 批准的 1,376 种药物进行筛选,发现了 格列美脲(非特异性 TRPM4 拮抗剂)、 环孢素 A(CsA)(线粒体通透性转换孔抑制剂)以及 二氢吡啶类(DHPs)钙通道阻滞剂 能够抑制NECSO。
但不同的是,CLT 直接靶向 TRPM4,竞争 NC1 结合口袋,抑制 TRPM4 活性,而DHPs 通过抑制 LTCCs(L 型钙通道)间接阻止 TRPM4 介导的 NECSO。
此外,研究还测试了 DHPs 和 CLT 对能量耗竭诱导的细胞死亡的抑制作用,发现这两种抑制剂在 Cos7 细胞中更有效地减少了 NC1 和能量耗竭诱导的 NECSO。它们还保护了表达 TRPM4 GOF 突变体的心肌母细胞免受能量耗竭的影响,表明 NECSO 抑制剂可能具有保护心脏细胞的治疗潜力,特别是在 TRPM4 GOF 突变的条件下。
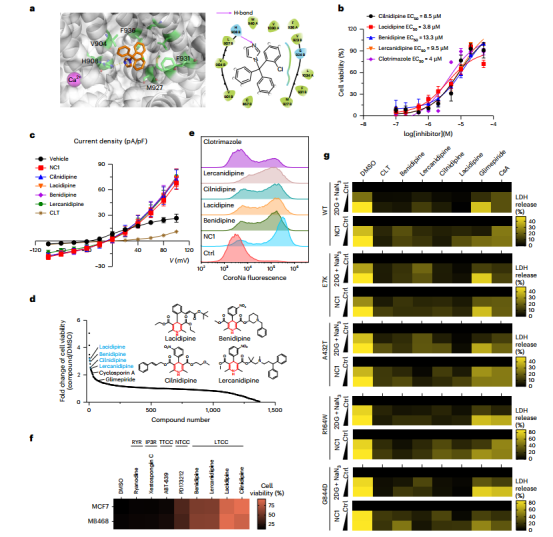
▲DHPs和CLT可作为NECSO的抑制剂
小结
综上,该研究报道了小分子化合物 NC1 诱导的一种特定类型的坏死性细胞死亡,并将其命名为钠过载细胞死亡(NECSO)。NECSO与凋亡(Apoptosis)、自噬(Autophagy) 及 已明确的程序性坏死(Programmed Necrosis) 途径均存在显著差异。其特征表现为 TRPM4 的持续激活导致其通道异常开放,引发大量钠离子内流和细胞膜去极化,最终导致坏死性细胞死亡。
此外,研究通过计算筛选和实验验证,鉴定了一系列能够抑制 NECSO 的小分子抑制剂,包括氯霉素(CLT)和二氢吡啶类(DHPs)。CLT 通过直接与 TRPM4 结合抑制其激活,而 DHPs 通过靶向 L 型钙通道(LTCCs)间接抑制 TRPM4 激活。这些抑制剂不仅能够抑制 NC1 诱导的细胞死亡,还能保护细胞免受能量耗竭诱导的坏死,在多种病理条件下显示出潜在的治疗应用价值。
往期推荐
1.Fu, W., Wang, J., Li, T. et al. Persistent activation of TRPM4 triggers necrotic cell death characterized by sodium overload. Nat Chem Biol (2025). https://doi.org/10.1038/s41589-025-01841-3





