
抗有丝分裂微管蛋白化合物库

Antimitotic Tubulin Library
产品编号DD1800
抗有丝分裂化合物库包含18,000种化合物。
微管是细胞骨架的核心组成部分,这种框架结构对维持细胞形态、细胞极性、细胞运动、信号传导、细胞分裂、细胞内运输及肌肉收缩等关键细胞过程至关重要。微管是由交替排列的α-和β-微管蛋白构成的中空圆柱形蛋白质结构,通过非共价键结合组装,其横截面包含13组并行的α/β-微管蛋白异二聚体。作为有丝分裂纺锤体的核心组分,微管在细胞增殖中发挥关键作用。构成有丝分裂纺锤体的动态微管是大多数抗有丝分裂剂的作用靶点。现有抗有丝分裂剂主要分为三大类:以紫杉烷类和埃博霉素类药物为主的微管稳定剂;作用于长春碱结合位点的微管蛋白聚合抑制剂;以及作用于秋水仙碱结合位点的微管蛋白聚合抑制剂。
目前已有数种成功的抗有丝分裂药物上市,大量化合物也正处于临床研发阶段,这类药物已成为抗癌疗法中的重要类别。然而,微管蛋白结合药物的临床应用受到多重因素制约:多药耐药性、不理想的药代动力学特性以及狭窄的治疗窗口。现有微管动力学调节剂还存在另一显著局限——临床疗效不足。尽管这类药物在体外实验中展现出卓越活性,但大多数微管蛋白结合剂在动物实验或临床环境中均未表现出显著的抗肿瘤效果。这种差异常归因于疗效与毒性间失衡(即治疗窗口狭窄),该平衡受药代动力学特性、脱靶毒性及其他尚未充分认知的因素影响。此外,药物外排泵也导致肿瘤对微管结合药物产生耐药性。因此,科研界持续需要靶向不同细胞内组分的新型调节剂,这类药物应能在实现传统微管结合抗有丝分裂效应的同时,不引发显著不良反应。例如驱动蛋白这类微管运动蛋白,它们在有丝分裂纺锤体功能中起关键作用,是新型癌症疗法开发的潜在靶点。其他调控有丝分裂进程的蛋白(如Polo、Bub、Mad、Aurora、Cdk1、分离酶等激酶与半胱氨酸蛋白酶)也为治疗干预提供了新途径。
产品编号DD1800
抗有丝分裂微管蛋白化合物库规格
- 1 mg
- 10 μL x 10 mM (in DMSO)
- 20 μL x 10 mM (in DMSO)
- 30 μL x 10 mM (in DMSO)
- 50 μL x 10 mM (in DMSO)
- 100 μL x 10 mM (in DMSO)
- 250 μL x 10 mM (in DMSO)
 产品描述
产品描述
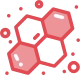
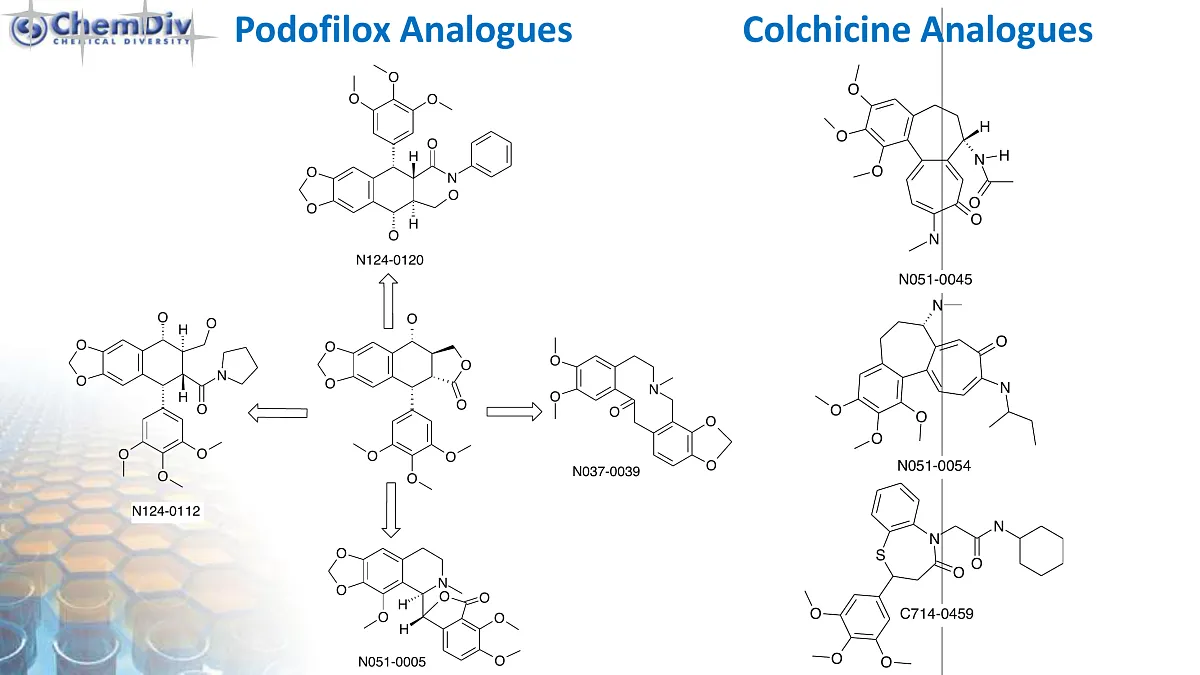
从研发历程看(见图1),研究人员主要聚焦两类抗有丝分裂药物:第一类是可逆结合微管蛋白、阻止微管组装与解聚的化合物(微管动力学调节剂);第二类是通过与特定细胞内靶点(如有丝分裂驱动蛋白、激酶、分离酶等)相互作用,间接调控有丝分裂事件的分子。
有丝分裂激酶
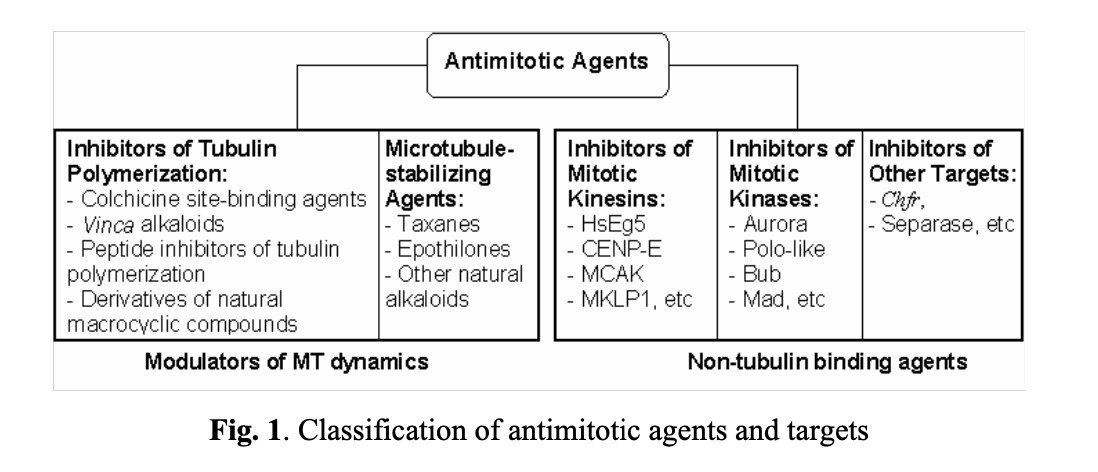
有丝分裂异常是导致遗传不稳定的关键因素之一,这种遗传不稳定是肿瘤发生的典型特征。临床证据表明,许多调控有丝分裂的蛋白质在人类肿瘤中存在异常表达。有丝分裂进程的调控依赖于两种翻译后机制,即蛋白质磷酸化和蛋白质水解。有丝分裂激酶介导蛋白质磷酸化,是控制有丝分裂进程的主要调控因子(表1)。
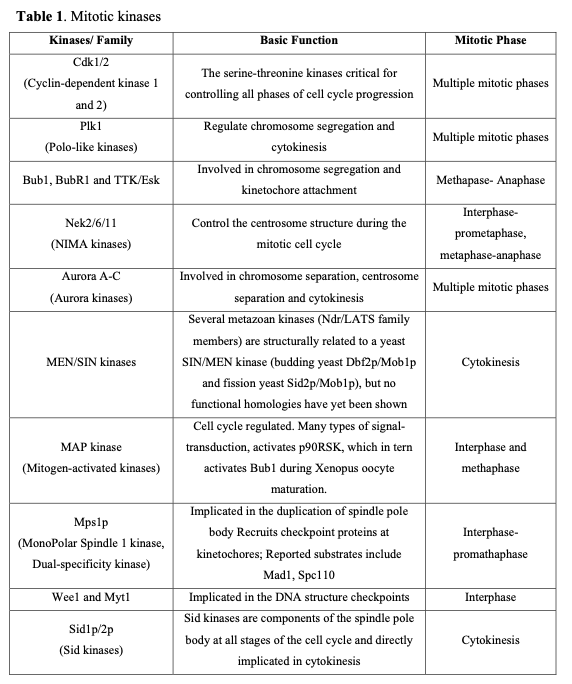
有丝分裂周期由四个主要阶段构成(见图2)。为确保子细胞获得完全相同的基因组副本,细胞周期进程受到一系列有丝分裂激酶的严格调控。其中最重要的Cdk1、Plk1和Nek2负责调控间期和前期的检查点机制。Cdk1在从前到末期的全过程发挥关键作用,而Aurora激酶对有丝分裂各阶段的细胞进程都至关重要。
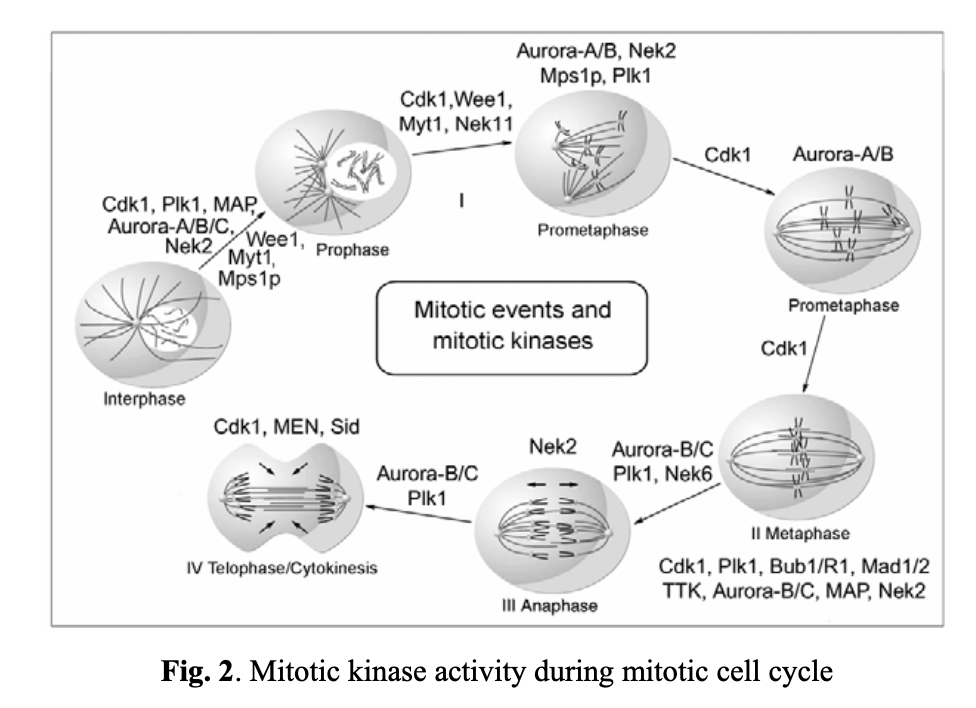
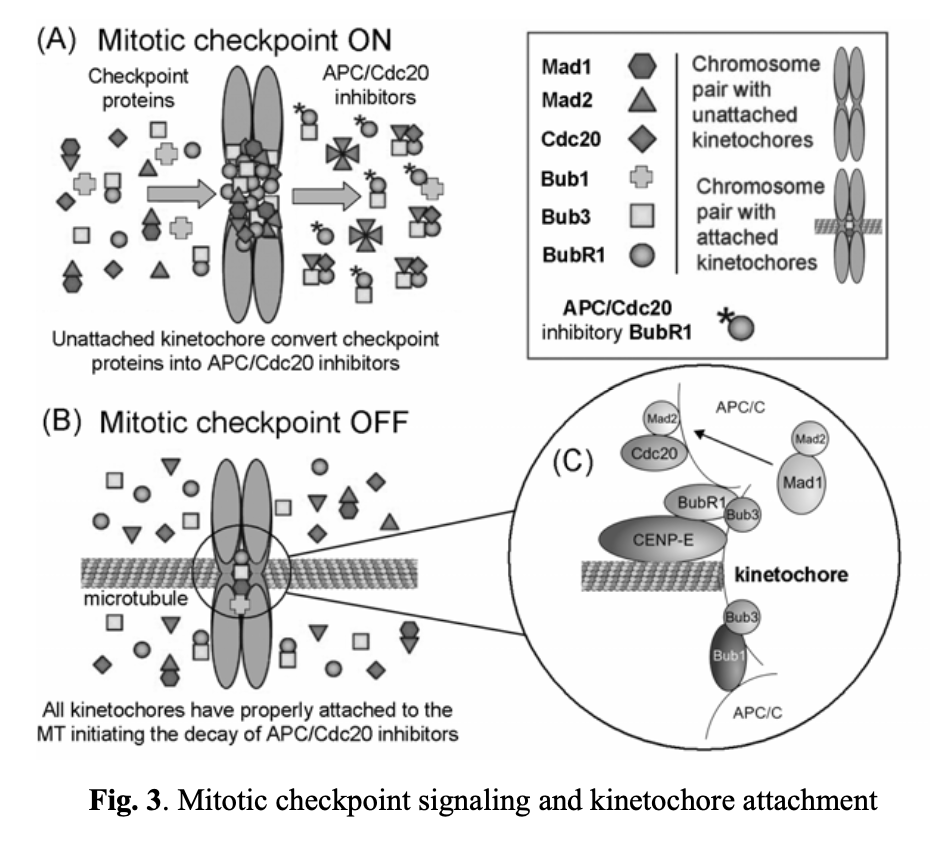
纺锤体组装检查点确保有丝分裂过程中染色体的准确分离。它会阻断分裂后期,直至所有染色体正确连接到双极有丝分裂纺锤体。当检测到不稳定染色体时,纺锤体检查点会抑制后期促进复合物/细胞周期体(APC/C)的泛素连接酶活性。这种抑制由BUB和MAD基因编码的蛋白质介导。具体而言,包括Bub1/3、BubR1、Bub3、Mad1和Mad2在内的有丝分裂激酶会被募集到未附着的动粒上(见图3)。DNA复制和中心体复制受E2F转录因子、Mps1p激酶、细胞周期蛋白A/E以及Cdc20蛋白调控。由BubR1、Bub3和Mad2组成的有丝分裂检查点蛋白复合物会结合并抑制APC/Cdc20,直至所有染色体正确附着于有丝分裂纺锤体并在赤道板上对齐(图3A、3B和3C)。
有丝分裂激酶的小分子抑制剂
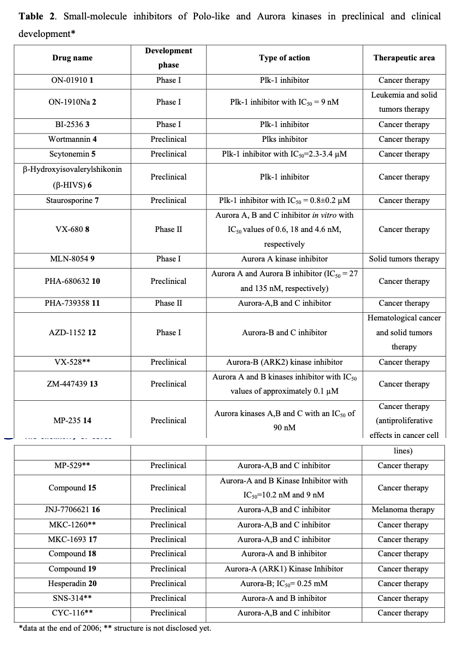
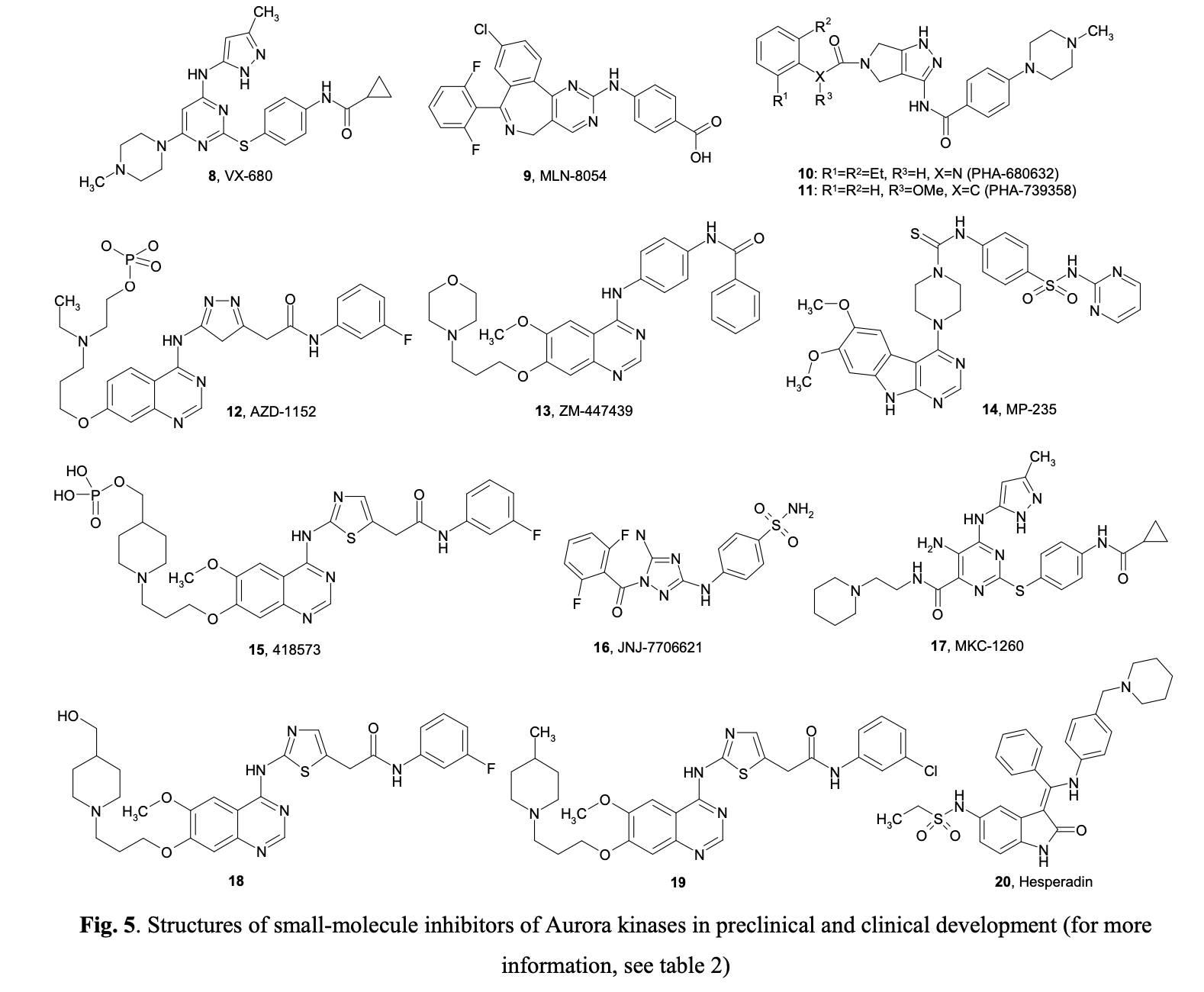
鉴于蛋白质磷酸化在有丝分裂检查点、纺锤体功能及染色体分离中的关键作用,多种有丝分裂激酶在肿瘤发生中的作用并不令人意外。例如,CDK1-8、极光激酶(AurA、AurB、AurC)、周期蛋白依赖性激酶(Cdk1、Cdk2)、Polo样激酶(Plk1-4)、Nek激酶(NIMA1-11)、Bub激酶(Bub1、BubR1)等均参与调控多种人类肿瘤的中心体复制、染色体分离与胞质分裂。这些激酶还调控中心体周期、纺锤体检查点、微管-动粒附着、纺锤体组装及染色体凝缩。目前已有多种高效且有选择性的有丝分裂激酶抑制剂进入临床试验阶段(见表2)。
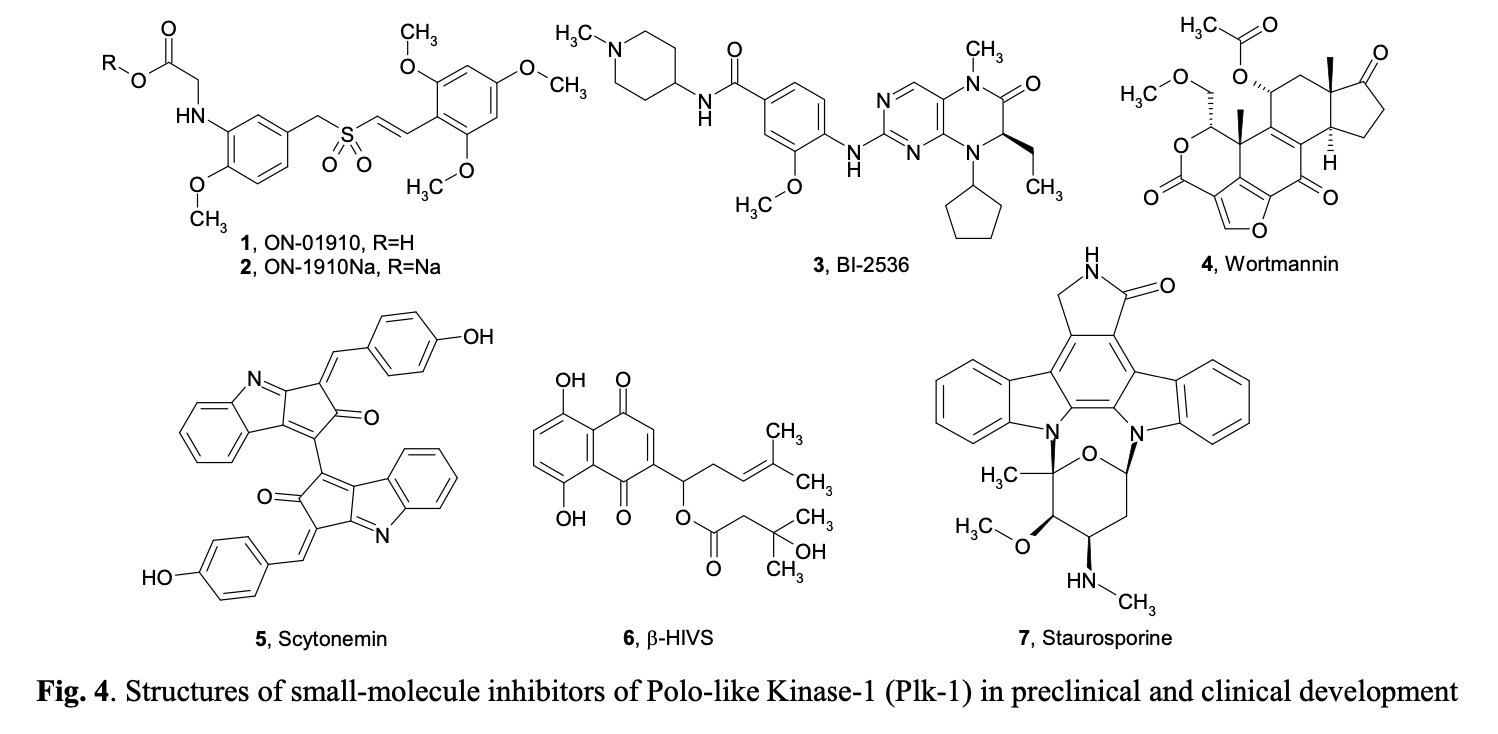
Polo样激酶抑制剂
Polo样激酶(Plks)属于一类保守的丝氨酸/苏氨酸激酶家族,其特征是含有一个Polo-box结构域。它们在细胞周期进程中具有相似但非冗余的功能,包括控制增殖细胞的进入有丝分裂,以及调节成功完成胞质分裂所需的各种有丝分裂因子。例如,它们对微管组织中心的活动至关重要,是细胞进入有丝分裂、纺锤体形成和胞质分裂的关键调控因子。在哺乳动物细胞中存在多种Plks(如Plk-1、Plk2/Snk、Plk3/Fnk/Prk和Plk4/Sak),非洲爪蟾中也存在同源物(Plx1-3)。在已知的四种人源Plk中,Plk-1在多种肿瘤类型中过度表达。在所有有丝分裂激酶中,Plk1的过表达尤为常见,这使其成为有丝分裂激酶中最受验证的靶点之一。实验结果表明,调节转化细胞和正常细胞中的Plk1活性具有抗增殖效应。Plks深度参与有丝分裂纺锤体装置的组装与动态调控,以及CDK/周期蛋白复合物的激活与失活。在哺乳动物细胞中,Plk1蛋白水平随细胞接近M期而升高,其磷酸化活性在分裂期达到峰值。已知的Plk1底物包括Cdc25C磷酸酶、周期蛋白B、有丝分裂纺锤体的黏连蛋白亚基、后期促进复合物的亚基以及哺乳动物驱动蛋白样蛋白1(MKLP-1)等其他驱动蛋白相关马达蛋白,这些底物凸显了Plk1在促进有丝分裂中的多层面作用。Plk1还通过磷酸化并激活Cdc25C来控制CDKs的酪氨酸去磷酸化。
经Plk抑制剂处理的癌细胞会走向凋亡或注定发生有丝分裂灾难。相反,非转化的增殖细胞会在G2/M期边界可逆性地停滞。小分子Plk抑制剂已显示出对癌细胞的选择性抗增殖作用,其产生的表型与Plks的已知功能一致。
极光激酶抑制剂
极光激酶家族的丝氨酸/苏氨酸蛋白激酶在所有真核生物的染色体分离和细胞分裂过程中起着关键作用。这类激酶最初在非洲爪蟾卵母细胞周期研究中被鉴定为Eg2蛋白,现已被确认为纺锤体检查点系统的重要组成部分,该系统可确保有丝分裂的准确性。极光激酶功能失调会破坏纺锤体组装、检查点功能和细胞分裂,导致染色体错误分离或多倍体化,并伴随中心体扩增。所有极光激酶都具有相似结构:其催化结构域两端分别连接极短的C端尾和长度可变的N端结构域。由于极光激酶在有丝分裂周期的多个阶段发挥调控作用(见图2),其作用靶点十分广泛。例如极光激酶A可磷酸化组蛋白H3(S10位点)、KSP驱动蛋白、CPEB、PP1、D-TACC及TPX2等多种底物;极光激酶B则调控组蛋白H3(S10/S28位点)、CENP-A、INCENP、REC-8、MgcRacGAP、波形蛋白、胶质纤维酸性蛋白、结蛋白等蛋白活性。极光激酶A自S期/早G2期定位于中心体,对建立双极有丝分裂纺锤体至关重要;极光激酶B在有丝分裂早期与染色体结合,后期从着丝粒迁移至纺锤体赤道板的微管上。随着纺锤体延伸和细胞进行胞质分裂,该激酶在纺锤体中间区富集,最终浓缩于中间体。极光激酶家族所有成员均特异性地在有丝分裂期表达。
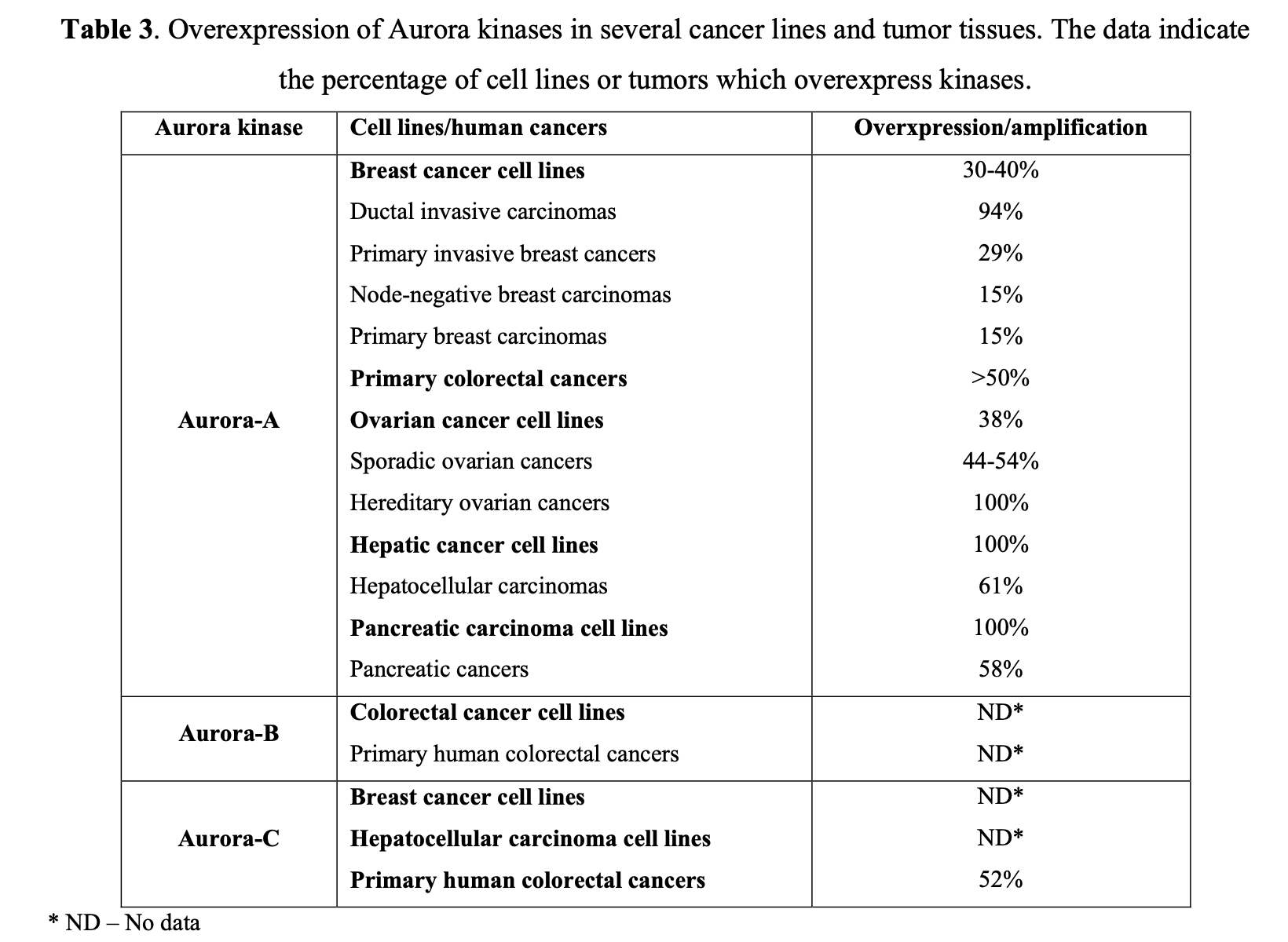
至少有极光激酶A和B两种亚型在人类肿瘤组织中普遍过表达,这在原发性结肠肿瘤样本中已得到证实。进一步研究表明,这两种激酶在乳腺癌、结直肠癌、膀胱癌和卵巢癌的发展过程中起关键作用(表3)。
细胞周期蛋白依赖性激酶(CDK)抑制剂
细胞周期蛋白依赖性激酶(CDKs)属于一个庞大的丝氨酸/苏氨酸激酶家族,在细胞周期调控,特别是有丝分裂早期阶段,发挥着至关重要的作用。它们也参与转录和mRNA加工的调控。然而,CDK9是一个例外,它不参与细胞周期调控。作为丝氨酸/苏氨酸激酶,CDKs能够磷酸化蛋白质上的丝氨酸和苏氨酸残基。一个细胞周期蛋白依赖性激酶通过与一个细胞周期蛋白结合形成复合体而被激活。CDK亚家族包括多个类别,命名为CDK1-9。细胞周期蛋白-CDK复合体通常受到多种激酶和磷酸酶的调控,包括Wee、CDK活化激酶(CAK)和Cdc25。CAK为复合体添加一个活化磷酸基团,而Wee则添加一个抑制性磷酸基团;同时存在活化和抑制性磷酸基团会使复合体处于失活状态。Cdc25是一种磷酸酶,能够去除Wee添加的抑制性磷酸基团,从而激活整个复合体。CDKs还会对Wee和Cdc25产生反馈,分别抑制和增强它们的活性。
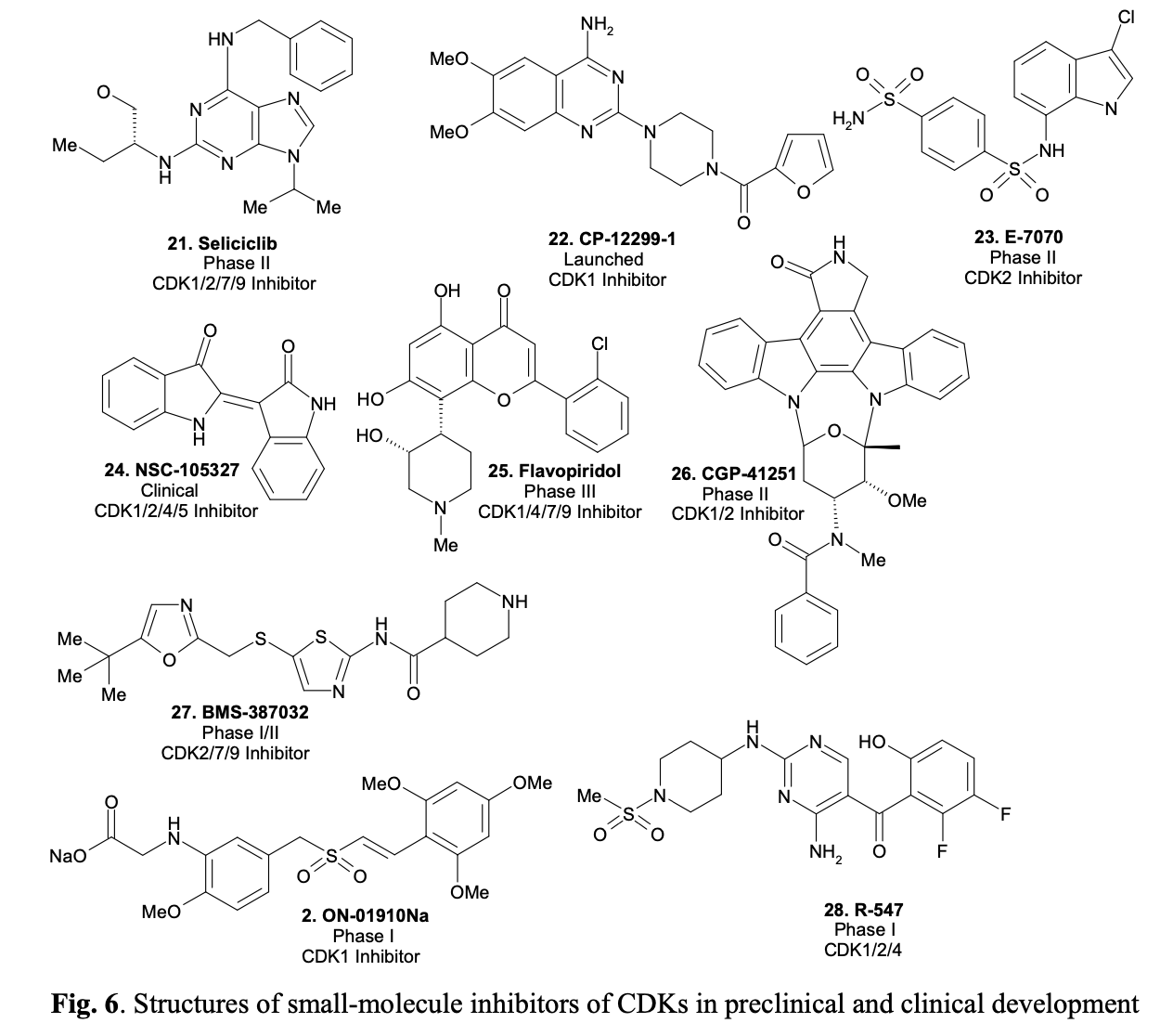
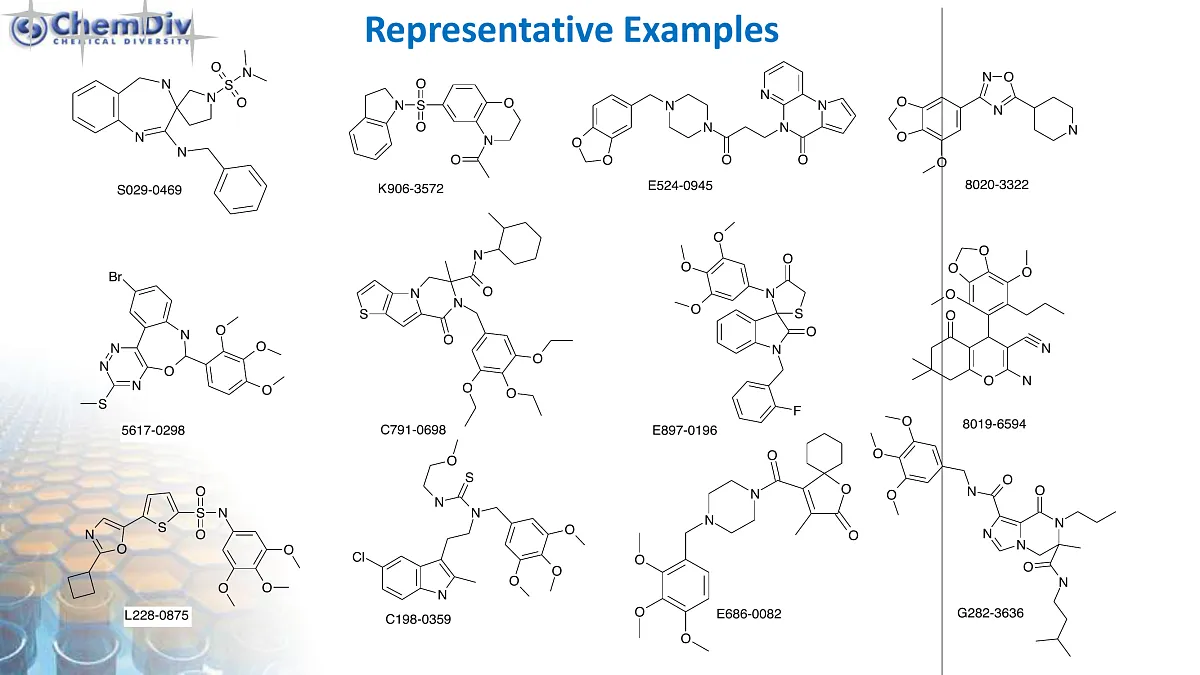
如今,CDKs被认为是抗癌治疗的潜在靶点。通过干扰CDK的作用,选择性地破坏癌细胞的细胞周期调控,可以靶向诱导这些细胞发生程序性死亡。目前,有几种CDK抑制剂正在进行临床试验,例如塞利西利。塞利西利(结构见图6)最初是作为一种潜在的抗癌药物被研发的,但最近的实验室测试表明,它还能诱导介导炎症的中性粒细胞凋亡。这一发现为开发治疗慢性炎症性疾病(如关节炎或囊性纤维化)的新型药物开辟了可能性。图6展示了处于临床前和临床试验阶段甚至已上市的小分子CDK抑制剂的代表性结构。


 包装和储存
包装和储存
- 可选用DMSO耐受的96/384孔板或2D 条形码编码管;
- 干粉蓝冰运输,DMSO溶液干冰运输;
- 排布:96孔板:1st & 12th 空白对照,384孔板:1st & 2nd & 23th & 24th空白对照。
 包装和储存
包装和储存
- 可选用DMSO耐受的96/384孔板或2D 条形码编码管;
- 干粉蓝冰运输,DMSO溶液干冰运输;
- 排布:96孔板:1st & 12th 空白对照,384孔板:1st & 2nd & 23th & 24th空白对照。
 化合物库定制
化合物库定制

 很棒
很棒